Autore: Ing. Giulia Veloce.
Nelle fasi di progettazione e realizzazione di ogni dispositivo medico, Leone ha sempre tenuto in primaria considerazione la sicurezza degli utilizzatori, cos├¼ come richiesto dalla Direttiva comunitaria sui dispositivi medici 93/42 e successive modificazioni. Essa infatti riporta i requisiti essenziali per la tutela della sicurezza di pazienti ed utilizzatori che un dispositivo medico deve rispettare affinch├® possa essere messo sul mercato. Da ci├▓ ne deriva che un prodotto pu├▓ essere commercializzato solo se viene sottoposto ad un adeguato processo di gestione del rischio, che pu├▓ essere conseguito secondo due modalit├á:
– tramite unÔÇÖanalisi qualitativa, seguendo una procedura fondata su unÔÇÖanalisi critica della letteratura scientifica pertinente, sulla esperienza del fabbricante, sulle prove effettuate e su tutte le indagini cliniche condotte;
– tramite unÔÇÖanalisi quantitativa che tenga conto delle eventuali norme tecniche esistenti.
Ambedue le analisi devono essere documentate in un apposito fascicolo tecnico, in continuo aggiornamento con dati derivanti dalla sorveglianza post-vendita, sempre a disposizione degli Organismi Notificati di sorveglianza e dellÔÇÖAutorit├á Competente che per lÔÇÖItalia ├¿ il Ministero della Salute.
Al momento dellÔÇÖavvio del progetto nel 2001, la scelta aziendale per lÔÇÖattivit├á di gestione del rischio del sistema implantare Leone ├¿ stata rivolta alla prima metodologia ed ha permesso di individuare gli elementi di potenziale rischio e attuare tutte le misure necessarie per minimizzarne gli effetti. Per poter avere un quadro completo e aggiornato del rischio ├¿ stato recentemente effettuato, in collaborazione con la Facolt├á di Ingegneria Biomedica dellÔÇÖUniversit├á degli Studi di Firenze, anche uno studio quantitativo che tenesse conto delle norme tecniche pi├╣ aggiornate.
Lo scopo era quello di evidenziare le differenze rispetto alla analisi qualitativa, con la possibilit├á di migliorare, eventualmente, il processo di gestione del rischio. Per far ci├▓, a partire dalla norma UNI CEI ISO 14971 (ÔÇ£Applicazione della gestione dei rischi per i dispositivi mediciÔÇØ) con lÔÇÖutilizzo di sofisticate metodologie quali la Failure Mode Effects Critically Analisys (FMECA), utilizzata da decenni in campo aeronautico e industriale e applicabile con successo in campo sanitario, sono state identificate le possibili fonti di pericolo, sono stati stimati i rischi associati allÔÇÖutilizzo del dispositivo medico, tenendo sempre in considerazione la valutazione del rapporto tra rischio e beneficio, ed infine, in base ai risultati ottenuti, ├¿ stato fatto un confronto con lÔÇÖanalisi dei rischi in essere.
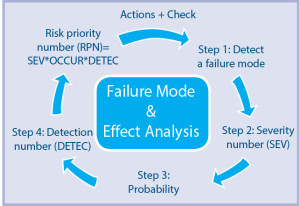
Il concetto di rischio ├¿ definito dalla norma come un fattore che tiene in considerazione la gravit├á del danno (Severity) causato da un potenziale evento negativo (Failure Mode) associato al dispositivo, la probabilit├á di accadimento dellÔÇÖevento negativo (Occurrence) e la capacit├á di identificare lÔÇÖevento negativo prima che esso si verifichi (Detection).
Questo studio quantitativo ha pienamente convalidato quanto affermato dalla originale valutazione del rischio secondo lÔÇÖapproccio qualitativo del sistema implantare Leone, confermandone dunque la validit├á anche dal punto di vista normativo e scientifico.
Da tale analisi ├¿ emerso inoltre come gli eventi negativi risultati pi├╣ critici siano connessi alla variabilit├á della parte clinica e dunque allÔÇÖutilizzo del prodotto. Ma ├¿ possibile determinare un parametro quantitativo che indichi lÔÇÖaffidabilit├á umana nellÔÇÖesecuzione di un dato compito? Per rispondere a questo quesito ├¿ stata approfondita la valutazione del rischio con innovative tecniche per lÔÇÖanalisi dellÔÇÖaffidabilit├á umana (Human Reliability Analysis). Tali tecniche sono nate in origine per settori come lÔÇÖaeronautico ed il nucleare per fornire valori di probabilit├á di errore connessi allÔÇÖoperato umano, con lo scopo di ridurre la probabilit├á di eventi incidentali.
Per quanto riguarda lÔÇÖambito degli impianti dentali, sono stati individuati vari parametri che descrivessero lÔÇÖaffidabilit├á correlata allÔÇÖazione di due categorie di utilizzatori e dunque ipotetiche fonti di errore: le figure professionali (medico e tecnico) ed il paziente.
LÔÇÖattivit├á di entrambi i professionisti ha grande influenza sullÔÇÖesito della riabilitazione implantoprotesica┬á ed in particolare si ├¿ concluso che le azioni che permettono di ridurre la probabilit├á di accadimento di un evento dannoso derivato da errore umano sono unÔÇÖadeguata formazione per le figure professionali ed una informazione che renda il paziente consapevole e attivo nelle varie fasi della gestione della riabilitazione.
A questo proposito la Società Leone svolge una intensa attività di informazione e formazione verso i clinici ed i tecnici tramite la propria divisione scientifica, Istituto Studi Odontoiatrici.
- Fig. 1 – Failure Mode Effects Critically Analysis (FMECA)
- Fig. 2 – Prova a flessione moncone temporaneo D 3,3