Autore:Â Prof. Guy Daculsi
MBCP+ è un fosfato di calcio bifasico composto da beta fosfato tricalcico (80%) e idrossiapatite (20%). La sua sicurezza ed efficacia nella rigenerazione ossea sono dimostrate da oltre 25 anni di studi preclinici e clinici. Le fondamentali prestazioni fisico-chimiche e biologiche di MBCP+ sono state studiate e documentate attraverso molteplici tecniche con più di 600 pubblicazioni. MBCP+ non è solo considerato il sostituto osseo ottimale per la rigenerazione ossea, ma anche l’impalcatura (scaffold) ideale per i nuovi biomateriali, come i sostituti ossei iniettabili e la combinazione con midollo osseo e con cellule staminali mesenchimali.
La rigenerazione ossea con MBCP+
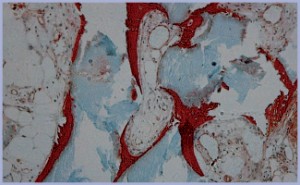
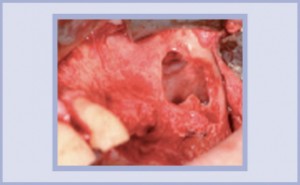
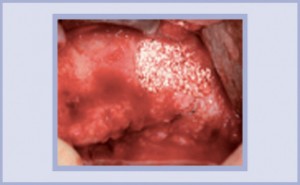
MBCP+ induce nelle cellule ossee, sia in vitro che in vivo, reazioni simili a quelle indotte da osso. Questo sostituto osseo permette l’adesione, la proliferazione e l’espressione cellulare. Dopo l’inserimento di MBCP+ in vivo, la prima attività biologica è la diffusione del fluido biologico, seguita dalla colonizzazione cellulare (Figg. 1-3).
- Figg. 1, 2, 3 – Subito dopo l’inserimento di MBCP+ in vivo: formazione di cristalli di apatite ossea nei micropori
- Fig. 2
- Fig. 3
L’idrossiapatite fa da impalcatura (scaffold) per la precipitazione dei cristalli ossei. Questi cristalli ossei neoformati hanno un’elevata area superficiale specifica e accumulano i fattori di crescita osteogenici del paziente. MBCP+ ha proprietà osteogeniche/osteoinduttive grazie alla natura chimica di idrossiapatite/fosfato tricalcico e alla particolare microstruttura (micropori) del materiale. Per questo motivo MBCP+ si riassorbe completamente e viene sostituito da osso ospite vitale (Fig. 4).
- Fig. 4 – Rigenerazione ossea nel rialzo del seno mascellare: istologia a 7 mesi dopo l’inserimento di MBCP+
Le differenze tra MBCP+ e altri materiali sintetici
I sostituti ossei sintetici sono in genere composti da fosfato tricalcico, idrossiapatite o una combinazione dei due. La capacità di riassorbimento (e quindi la dissoluzione in vivo) di questi materiali dipende in parte dal loro rapporto di beta fosfato tricalcico/idrossiapatite: poiché il beta fosfato tricalcico è più solubile dell’idrossiapatite, la capacità di riassorbimento del sostituto osseo sintetico è proporzionale alla percentuale di beta fosfato tricalcico in esso contenuto. Dissoluzione, proliferazione cellulare e crescita di osso all’interno del materiale dipendono però anche dal processo di sinterizzazione. Studi recenti dimostrano che il riassorbimento dei fosfati di calcio bifasici e la crescita ossea all’interno del materiale sono direttamente correlati alla temperatura di sinterizzazione: più alta è la temperatura di sinterizzazione, più bassa è la percentuale di microporosità e più bassa è la capacità di riassorbimento e di crescita ossea all’interno del biomateriale. Questi studi provano che una microporosità e un’area superficiale specifica ideale inducono un’ottima risposta cellulare e incidono in modo significativo sulla capacità di crescita ossea all’interno del materiale. MBCP+ soddisfa queste specifiche: ottimo rapporto betafosfato tricalcico/idrossiapatite, oltre 30% di microporosità per la precipitazione dei cristalli ossei, un’elevata area di superficie specifica per la dissoluzione, il riassorbimento e la crescita ossea all’interno del materiale in sostituzione del fosfato di calcio bifasico micro e macroporoso (Figg. 5-7).1, 2
- Fig. 5 – MBCP+: oltre 30% di microporosità (copertura cellulare 36% +/- 1.6)
- Fig. 6, 7 – Altri sostituti ossei sintetici: meno del 10% di microporosità (copertura cellulare 16% +/- 2.0)
- Fig. 7
Le differenze tra MBCP+ e xenoinnesti di origine bovina
Gli xenoinnesti di origine bovina possono essere morfologicamente simili all’osso umano, ma non contengono alcun potenziale osteoinduttivo. Nella maggior parte dei casi non si riassorbono e rimangono incapsulati nell’innesto come particelle murate nell’osso ospite. Uno studio recente paragona il risultato di interventi di rialzo del seno mascellare effettuati con MBCP+ con altri effettuati con Bio-Oss® (Geistlich) attraverso biopsie ossee realizzate durante la preparazione del sito implantare. Le biopsie sono state analizzate in istologie classiche senza decalcificazione e attraverso ricostruzioni 3D utilizzando micro CT. Il riempimento osseo del seno mascellare realizzato con MBCP+ dimostra dopo 6 – 8 mesi una sufficiente crescita ossea al suo interno per dare supporto a impianti dentali (Figg. 10, 11).
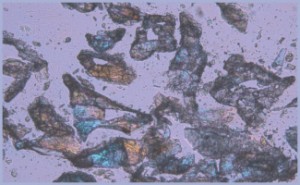
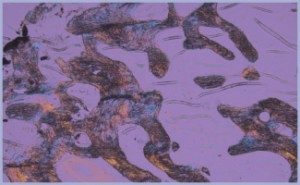
Le istologie e i micro CT ottenuti dalle biopsie avvenute prima dell’inserimento implantare rivelano un’elevata crescita ossea all’interno del materiale e un’architettura ossea adatta per dare stabilità meccanica durante la fase di osteointegrazione. Per Bio-Oss® (Geistlich), dopo 6 mesi dall’inserimento, non si osservano invece alcun riassorbimento e alcuna crescita di osso all’interno del materiale, nonostante una buona efficacia clinica (Figg. 8, 9).3
- Fig. 8 – Microscopio a luce: Bio-Oss® a 6 mesi dal suo inserimento non si osserva alcuna crescita ossea al suo interno; nero: granuli Bio-Oss® intatti; viola: formazione di nuovo osso soltanto intorno ai granuli
- Fig. 9 – Microscopio polarizzatore: MBCP+ a 6 mesi dal suo inserimento si osservano granuli in processo di riassorbimento; nero: granuli parzialmente riassorbiti con crescita ossea al loro interno; viola: formazione di nuovo osso in sostituzione di MBCP+
- Figg. 10, 11 – Rialzo del seno mascellare (Dr. Malhac – Francia); riempimento del seno mascellare con MBCP+ e inserimento degli impianti dopo 6 mesi
- Fig. 11
Caso 1
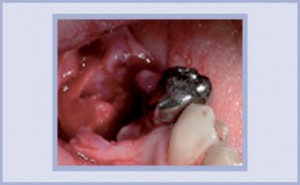
Rialzo del seno mascellare prima dell’inserimento di impianti
Ospedale universitario CHU Nantes, Francia (figg. 12-19)
- Il paziente ha chiesto un restauro protesico fisso. Nel settore II è stato pianificato il trattamento implantoprotesico.
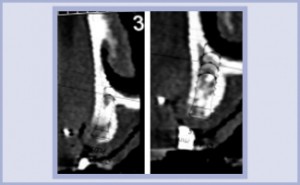
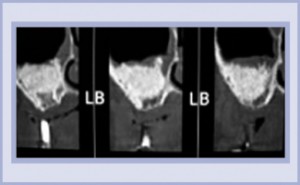
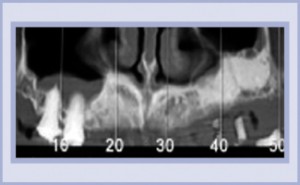
- Le immagini TC pre-operative confermano la mancanza di volume osseo nel seno mascellare (circa 2 e 5 mm). Problema osservato: forte riassorbimento dell’osso mascellare e incremento del volume del seno mascellare che richiedono un intervento di rigenerazione ossea prima di poter posizionare gli impianti. Decisione terapeutica: riempimento del seno mascellare con granuli di MBCP+.
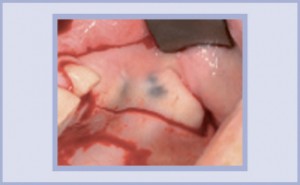
- Immagine clinica dell’area interessata al rialzo del seno con incisione crestale.
- Apertura di una finestra laterale al seno mascellare e sollevamento della membrana sinusale.
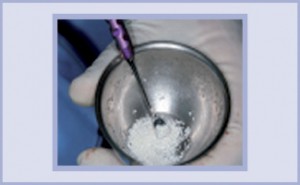
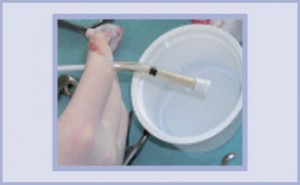
- Preparazione dei granuli MBCP+ 1-2 mm in una vaschetta. I granuli MBCP+ sono inumiditi con soluzione fisiologica senza effettuare alcuna pressione sui granuli per preservare la loro specifica microstruttura. In caso di insufficiente vascolarizzazione del seno, dopo averli inumiditi con soluzione fisiologica, si mischiano con sangue del paziente.
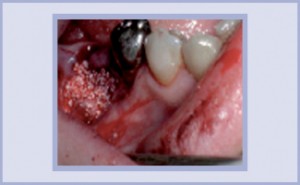
- Applicazione di MBCP+ nel seno mascellare senza alcuna compattazione, in modo da mantenere lo spazio tra i granuli per permettere la completa vascolarizzazione del materiale. I micropori saranno colonizzati dalle cellule del paziente per dare inizio al processo di riassorbimento con progressiva sostituzione con osso neoformato. L’innesto osseo è coperto da EZ Cure, una membrana di collagene riassorbibile e si suturano i lembi gengivali sopra la membrana a copertura del sito.
- Le immagini TC a 7 mesi dall’intervento rivelano che l’altezza dell’osso è preservata. MBCP+ si sta progressivamente trasformando in nuovo osso con una resistenza meccanica sufficiente per l’inserimento implantare.
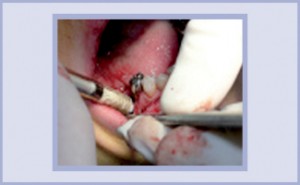
- A 7 mesi dall’intervento si posizionano gli impianti nell’area della rigenerazione ossea.
Diversi studi dimostrano che MBCP+ utilizzato come sostituto osseo nel rialzo del seno mascellare, da solo o in combinazione con altri materiali osteoinduttivi, porta a risultati predicibili per l’inserimento di impianti dentali nella zona del mascellare posteriore superiore con insufficiente altezza verticale per il posizionamento implantare.4, 5
Caso 2
Preservazione della cresta ossea per il futuro inserimento implantare
Ospedale universitario CHU Nantes, Francia (figg. 20-28)
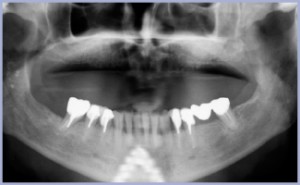
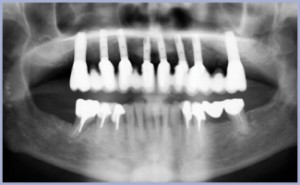
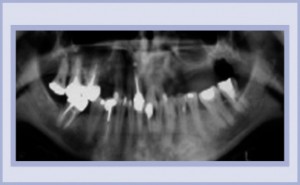
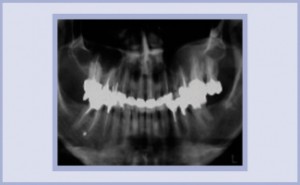
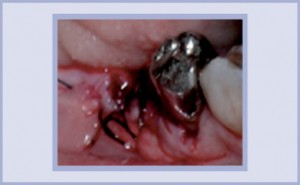
- OPT pre-operativa: è necessario estrarre il 46.
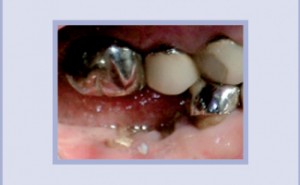
- Esame endo-buccale: parodontite stabilizzata. Area da trattare: gengiva cheratinizzata con poco spessore, nessun dolore alla palpazione.
- Incisione e apertura del lembo; estrazione del dente; revisione e curettage dell’alveolo.
- Preparazione dei granuli MBCP+ 0,5-1 mm: si inumidiscono i granuli aspirando soluzione fisiologica attraverso il cappuccio-filtro della siringa.
- Si applicano i granuli MBCP+ nel difetto per mezzo della siringa, dopo aver rimosso il cappuccio-filtro, senza alcuna compattazione e senza sovrariempire il sito, in modo da preservare la microstuttura dei granuli e permettere la veloce vascolarizzazione dei granuli MBCP+.
- Si rimuovono i granuli in eccesso. Non compattare mai i granuli premendoli con strumenti/osteotomi al fine di preservare la permeabilità del materiale e permettere la diffusione dei fluidi biologici del paziente.
- Copertura con un innesto di tessuto molle e sutura.
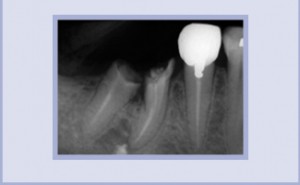
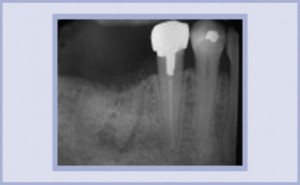
- La radiografia di controllo a 6 mesi evidenzia una buona rigenerazione ossea. L’impianto può essere inserito.
Bibliografia
(1)Daculsi G, Laboux O , Malard O, Weiss P. Current state of the art of biphasic calcium phosphate bioceramics. Journal of materials science 2003: materials in medicine, vol 14 (3): 195-200
(2)Daculsi G, LeGeros R Z, Grimandi G, Soueidan A, Aguado E, Goyenvalle E, LeGeros J. Effect of Sintering Process of HA/TCP Bioceramics on Microstructure, Dissolution, Cell Proliferation and Bone Ingrowth. Key Engineering materials 2008, vols 361-363: 1139-1142
(3)Malard O, Gauthier H, Daculsi G. In vivo demonstration of 2 types of microporosity on the kinetic of bone ingrowth and biphasic calcium phosphate bioceramics resorption; Key engineering materials 2008, vols 361-363: 1233-1236
(4)Mailhac N, Daculsi G. Bone Ingrowth for Sinus Lift Augmentation with Micro Macroporous Biphasic Calcium Human Cases Evaluation – Using MicroCT and Histomorphometry Clinique Dentaire, Nantes University ERT 1051, Faculty of dental Surgery, Place A. Ricordeau, 44042 Nantes Cedex
(5)Lee J H, Jung U W, Kim C S, Choi S H, Cho K S, Histologic and clinical evaluation for maxillary sinus augmentation using macroporous biphasic calcium phosphate in human, Clin Oral Impl Res 19, 2008, 19, 767-771